Новые синтетические методы, основанные на сольвотермическом подходе, такие как ионотермические процессы, были использованы для получения нанопорошков LiMPO4 (M = Mn, Co и Ni), LixMSiO4 [Nytén, A. et al. (2005)] и материалы для батарей на основе фторфосфатов лития и натрия [DiSalvo, FJ et al.
(1971); Эллис, Б.Л. и др. (2007b)] с использованием низкой температуры нагрева. Ионотермический синтез возник, когда большой объем исследовательской работы был направлен на поиск новых недорогих процессов изготовления электродных материалов с высокой электрохимической оптимизацией. Этот альтернативный путь считается новым недорогим процессом синтеза, поскольку он требует гораздо меньше энергии, чем способы высокотемпературной керамики. Несмотря на более высокую стоимость ионных жидкостей по сравнению с водой, доказано, что эти растворители можно использовать повторно без очистки при использовании для приготовления одного и того же материала, что приводит к значительному снижению стоимости и минимизации образования отходов [Tarascon, JM. и другие. (2010)]. Ионотермический синтез также успешно осуществляется с использованием микроволнового излучения, а не традиционного нагрева, что сокращает время реакции и необходимую энергию для синтеза.
Ионотермический синтез основан на использовании в качестве реагирующей среды вместо воды в сольвотермических условиях ионной жидкости. Ионные жидкости представляют собой класс органических растворителей с высокой полярностью и заранее организованной структурой растворителя [Дель Пополо, М.Г. и Вот, Г.А. (2004)]. Ионные жидкости комнатной температуры (или температуры, близкой к комнатной) классически определяются как жидкости при температуре окружающей среды (или <100 ° C), состоящие из органических катионов и анионов.
Они обладают превосходными сольватирующими свойствами, малоизмеримым давлением пара и высокой термической стабильностью. Сольватирующие свойства и температура плавления будут зависеть от выбранной комбинации катионов и анионов. В области материаловедения было несколько сообщений об использовании ионных жидкостей в качестве растворителей с очень небольшим или контролируемым количеством воды, участвующей в синтезе [Antonietti, M et al. (2004)]. Большинство этих исследований было сосредоточено на аморфных материалах и наноматериалах.
Как и вода, ионные жидкости, образующиеся из совместимых катионных/анионных пар, обладают превосходными растворяющими свойствами. Кроме того, они обладают высокой термической стабильностью и незначительной летучестью, поэтому использование автоклава не является обязательным. Более того, из-за гибкой природы катионных/анионных пар они, как растворители, предоставляют большие возможности для целенаправленного управления зародышеобразованием. За последнее десятилетие ионотермический синтез превратился в выгодный синтетический метод получения зеотипов [Lin, ZJ. и другие. (2008)] и другие пористые материалы, такие как металлоорганические каркасные соединения (MOF), но этот метод очень ограниченно использовался в синтезе неорганических соединений.
Уникальной особенностью ионотермического синтеза является то, что ионная жидкость действует одновременно как растворитель и поставщик шаблона. Многие катионы ионных жидкостей химически очень похожи на виды, которые уже известны как хорошие темплаты (ионные жидкости на основе алкилимидазолия, пиридиния). Многие из них являются относительно полярными растворителями, что делает их пригодными для растворения неорганических компонентов, необходимых для синтеза. Одним из определяющих свойств ионных жидкостей является отсутствие у них обнаруживаемого давления пара, что эффективно приводит к устранению проблем безопасности, связанных с высокими гидротермальными давлениями, а также привело к их использованию в микроволновом синтезе.
В процессе ионотермического пути, поскольку в реакционную смесь не добавляются другие растворители, теория утверждает, что никакие другие молекулы не присутствуют в качестве наполнителей пространства во время синтеза. Это означает, что ионотермический метод идеально устраняет конкуренцию между взаимодействиями темплат-каркас и растворитель-каркас, присутствующую в гидротермальных препаратах. Однако это идеалистический сценарий, который не всегда достижим из-за возможного разложения небольшой доли катионов ионной жидкости, что приводит к образованию более мелких катионов-шаблонов, которые могут преимущественно действовать как структурообразующий агент в растворителе ионной жидкости [Парнхем , ER и Моррис, RE (2006)].
Недавние исследования молекулярного моделирования показывают, что структуры ионных жидкостей характеризуются дальнодействующими корреляциями и распределениями, которые отражают асимметричные структуры катионов. Асимметричные эффекты такого рода на большом расстоянии потенциально увеличивают вероятность передачи химической информации от матричного катиона к каркасу, что желательно, если необходимо достичь полного контроля над процессом шаблонизации [Parnham, ER and Morris, RE (2007). )].
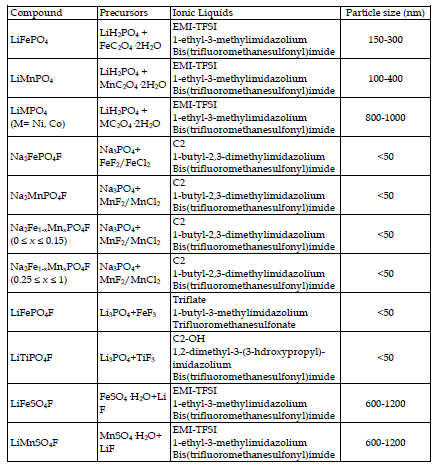
Тараскон и др. были первыми, кто применил ионотермический синтез к материалам аккумуляторных электродов. Они протестировали несколько ионных жидкостей на основе различных катионных и анионных частиц в качестве реакционной среды для приготовления фазы LiFePO4 [Recham, N. et al. (2009а)]. Используемые ионные жидкости продемонстрировали влияние на зародышеобразование/рост LiFePO4 и действуют как структурно-направляющий агент. Например, использование ионной жидкости EMI-TFSI с функционалом CN [бис(трифторметансульфонил)имид 1-этил-3-метилимидазолия] привело к образованию игольчатых порошков в направлении [010], которые идеально складывались в кучу, образуя иглу большего размера. Это изменение концевой группы изменило полярный характер реагирующей среды и ее сольватирующие свойства, тем самым влияя на рост кристаллов. Тромбоцитоподобные частицы вдоль направления [020] были созданы за счет уменьшения полярности за счет использования катиона EMI на основе C18. Образование этих
двух морфологических видов можно объяснить конкурирующими энергетическими поверхностями и напрямую связано с природой ионной жидкости, сольватирующей способностью, полярностью и способностью специфически поглощать на одной из поверхностей. В зависимости от свойств ионной жидкости минимизация поверхностной энергии системы будет происходить по разному механизму. Все произведенные материалы LiFePO4 были электрохимически активными, но с лучшими характеристиками имели размеры 300 и 500 нм, демонстрируя удельную емкость 150 мАч·г-1 при C/10 без углеродного покрытия.
Ионотермический процесс был распространен на синтез фторфосфатов на основе Na с контролируемым размером [Na2MPO4F (M = Fe, Mn)] [Recham, N. et al. (2009б)]. Эти фазы являются привлекательными электродными материалами, поскольку они основаны на экономичных металлах и могут использоваться как в батареях на основе лития, так и в батареях на основе натрия. Кроме того, фториды обладают более высокой электроотрицательностью, что увеличивает ионность связей и, следовательно, их окислительно-восстановительный потенциал за счет индуктивного эффекта. Наноразмерные образцы Na2FePO4F и Na2MnPO4F диаметром около 25 нм были приготовлены в ионной жидкости бис(трифторметансульфонилимида) 1,2-диметил-3-бутилимидазолия, в отличие от крупнозернистых порошков, полученных керамическим методом. Электрохимические характеристики соединения железа достигли лучших результатов, чем у керамического материала: 115 мАч·г-1, лучшая начальная емкость, меньшая необратимая емкость, меньшая поляризация и лучшее сохранение емкости. Марганцевая фаза не проявляла электрохимической активности, что соответствует общей тенденции соединений на основе Mn, имеющих худшие электрохимические характеристики, чем их Fe-аналог, например, в семействах LiMPO4 и Li2MSiO4. С этим явлением связаны два фактора. Во-первых, сильное ян-теллеровское искажение на Mn3+, влияющее на его координационную сферу; во-вторых, плохая электронно-ионная проводимость материалов из-за большей ионности МО-связи.
Ионотермический процесс успешно применяется для получения новых, ранее не известных электроактивных материалов, таких как LiFeSO4F. Этот материал обладает адекватной структурой, способствующей миграции ионов лития по каналам. Эту электроактивную фазу ранее не синтезировали, поскольку она недоступна ни керамическим способом, ни в водной среде. Разлагается при температуре выше 375°С и в водной среде. Этот новый катодный материал показал электрохимическую активность при напряжении 3,6 В и обратимую удельную емкость 140 мАч·г-1, что очень близко к теоретическому значению удельной емкости 151 мАч·г-1. Таким образом, этот препаративный процесс оказался полезным инструментом для синтеза наноразмерных новых и известных электроактивных материалов.
